MISURARE LA DENSITA’: come procedere
Come accennato, i solidi sono più densi dei liquidi, che a loro volta risultano più densi dei gas. Inoltre dobbiamo ricordare che le sostanze gassose si comprimono e si espandono anche notevolmente al variare di pressione e temperatura. Di conseguenza la loro densità dipende da TEMPERATURA e PRESSIONE, che di solito viene misurata in quelle che i chimici definiscono “CONDIZIONI STANDARD”, ovvero a 0°C e alla pressione di 1 atm.
Avrete capito quindi che per misurare la densità procederemo in maniera diversa a seconda che si tratti di un solido di un liquido o di un gas. Vediamo quindi come agire nelle tre situazioni
⇒ CALCOLO DELLA DENSITA’ DI UN SOLIDO
Dobbiamo distinguere due casi, a seconda che il solido sia REGOLARE oppure no
- Se conosciamo la formula per calcolare del volume del solido:
- misuriamo le dimensioni del solido: altezza, larghezza e lunghezza
- calcoliamo il volume V secondo la sua forma (cubo, sfera, cilindro…)
- misuriamo la massa m del solido mediante una bilancia;
- calcoliamo infine la densità del solido con la formula
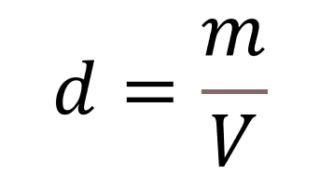
- Se non conosciamo la formula per calcolare il volume del nostro oggetto
- misuriamo il volume del solido immergendo il corpo in un cilindro graduato contenente acqua. Leggiamo innanzitutto il VOLUME INIZIALE dell’acqua e poi il VOLUME FINALE dopo aver messo l’oggetto nel cilindro. Otteniamo il volume del solido come DIFFERENZA tra il volume finale e quello iniziale:
 V = Vfin – Vin
V = Vfin – Vin
- misuriamo la massa m del corpo mediante una bilancia;
- calcoliamo infine la densità con la formula d = m/V
⇒ CALCOLO DELLA DENSITA’ DI UN LIQUIDO
Se dobbiamo misurare la densità di un liquido procediamo nel modo seguente :
- versiamo il liquido in un cilindro graduato;
- misuriamo il volume V che il liquido occupa;
- misuriamo la massa del cilindro con il liquido (m1);
- misuriamo la massa del cilindro vuoto (m2);
- ricaviamo la massa del liquido : m = m1–m2 ;
- calcoliamo infine la densità del liquido mediante la formula: d = m/V
⇒ CALCOLO DELLA DENSITA’ DI UN GAS
Per misurare la densità di un gas dovremo seguire una procedura analoga a quella utilizzata per il calcolo della densità dei liquidi.
In questo caso però dobbiamo avere ben presente che la densità dei gas DIPENDE da PRESSIONE e TEMPERATURA. Infatti i gas si comprimono e si espandono notevolmente al variare di temperatura e pressione. Solitamente la densità dei gas viene misurata in quelle che i chimici chiamano “CONDIZIONI NORMALI”, cioè a T = 0°C (273 K) e P= 1 atm (cioè la pressione atmosferica media a livello del mare)
A PROPOSITO DI CONDIZIONI NORMALI: Nell’espressione “condizioni normali”, il termine normale significa normalizzato e non usuale.
Agli inizi del XIX secolo, per lo studio dei gas i fisici si sono resi conto che era necessario riferire i risultati dei loro esperimenti a condizioni standard di pressione e temperatura. I valori fissati derivano da un accordo tra sperimentatori legato soprattutto alla consuetudine.
MISURARE LA DENSITA’ per smascherare i falsari
Nel III secolo a.C., il tiranno di Siracusa Gerone II si fece realizzare una corona da un orafo ma volle assicurarsi che fosse davvero di oro puro. Si rivolse perciò al suo amico Archimede, che risolse il problema utilizzando semplicemente una bilancia e una bacinella d’acqua.
Mise la corona su un piatto della bilancia e pose sull’altro piatto un pezzo di oro puro con la stessa massa della corona, portando così la bilancia in equilibrio. Fece quindi lo stesso con un pezzo d’argento avente la stessa massa della corona.

Immerse poi uno alla volta gli oggetti in un recipiente pieno di acqua e vide che i volumi erano DIVERSI. Da questo dedusse che l’orafo avesse sostituito parte dell’oro con argento. Infatti se la corona fosse stata di oro puro, avrebbe avuto la stessa densità dell’oggetto di oro puro, che nel SI è pari a 19 300 kg/m³.
Siccome la massa era la stessa, anche il volume avrebbe dovuto essere uguale. Ricordiamo infatti che
V = m/d
Siccome i volumi erano diversi, i due oggetti non potevano essere fatti dello stesso materiale! Proprio grazie a questo quesito il grande scienziato ebbe l’intuizione per il suo PRINCIPIO: un corpo immerso in un fluido riceve una spinta dal basso verso l’alto pari al volume di fluido spostato. E il volume di fluido spostato è UGUALE al volume del corpo immerso.
Immergendosi in una vasca, notò che, mentre il suo corpo affondava, il livello dell’acqua saliva. Questo gli diede l’idea per risolvere il problema che lo assillava da quando Gerone glielo aveva presentato.
Riempì quindi di acqua un contenitore e vi immerse un oggetto di oro puro con lo stesso peso della corona. Raccolse l’acqua traboccata, il cui volume era pari al volume dell’oggetto. Immerse quindi nel contenitore un oggetto d’argento dello stesso peso della corona e vide che la quantità di acqua traboccata era maggiore di quella versata con l’oggetto d’oro.
Infatti l’oro ha densità maggiore dell’argento ed occupa quindi un volume minore.
Ripeté infine il procedimento con la corona. Anche in questo caso la quantità di acqua traboccata era maggiore di quella versata dopo aver immerso l’oggetto d’oro puro ma risultava MINORE di quella tracimata dopo aver immerso l’oggetto d’argento. Da questo Archimede dedusse che l’orafo aveva sostituito parte dell’oro con argento

MISURARE LA DENSITA’ : bibliografia
- Ugo Amaldi – Il nuovo Amaldi per i licei scientifici. Meccanica e termodinamica (Vol. 1) Zanichelli, 2021
- Giuseppe Ruffo, Nunzio Lanotte – Fisica: lezioni e problemi. Meccanica, termodinamica, onde, elettromagnetismo, Zanichelli 2021
- James S. Walker – Il Walker. Corso di fisica. Per il primo biennio delle Scuole superiori, Pearson 2021
- Andrea Brognara – Lo sguardo fisico, Mondadori Scuola, 2019